Durch eine Schieflage in der Wasserchemie kann es zu einer Ammoniakvergiftung von Fischen kommen. Diese erkennt man an Atemproblemen, geringerer Futteraufnahme und daran, dass die Fische apathisch wirken.
Die FischhalterInnen unter Ihnen haben sicher schon davon gehört, dass es unter gewissen Umständen zu der Freisetzung von giftigem Ammoniak im Wasser kommen kann. Je nach Ausmaß reichen die Folgen von einer Reizung der Kiemen bis zum Tod der Fische. Dies betrifft sowohl Aquarien als auch Fischteiche und andere Fischzucht- und mastanlagen. In diesem Blogbeitrag möchte ich erklären, wie es chemisch gesehen zu diesem kritischen Zustand kommt, damit Sie in Zukunft das Wohlbefinden Ihrer Schützlinge sicherstellen können und eine Ammoniakvergiftung der Fische vermieden werden kann.
Was ist Ammoniak?
Ammoniak ist eigentlich ein Gas, das aus einem Stickstoff- und drei Wasserstoffatomen besteht. Die chemische Formel lautet NH3. Kommt es in Kontakt mit Wasser, stellt sich ein Gleichgewicht zwischen Ammoniak und Ammonium-Ionen (NH4+) ein:
NH3 + H2O ⇌ NH4+ + OH–
Weil solche Reaktionsgleichungen unter Umständen abschreckend auf den/die BetrachterIn wirken können, will ich in Worten die Reaktion beschreiben – man spricht also:
Ammoniak (NH3) reagiert mit Wasser (H2O) im Gleichgewicht (⇌) zu Ammonium (NH4+)- und Hydroxid (OH–)-Ionen.
Wobei die Hydroxid-Ionen die Träger der basischen Eigenschaft einer Lösung sind. Beim Lösen von Ammoniak in reinem Wasser wird also der pH-Wert erhöht (Ihnen ist gerade nicht mehr ganz klar, was der pH-Wert ist? – kein Problem, schauen einfach in meinen Beitrag dazu rein).
Das heißt beispielsweise, wenn wir den Gehalt einer Produktspezies (zum Beispiel das Hydroxid-Ion) verringern, wird das Gleichgewicht versuchen, dieses Defizit auszugleichen. Die Reaktion wird dann nach obiger Schreibweise vermehrt nach rechts ablaufen. Dies hat zur Folge, dass effektiv weniger Ammoniak und dafür mehr Ammonium vorliegt.
Damit haben wir auch schon die erste Variante erarbeitet, wie man einem zu hohen Ammoniakgehalt entgegenwirken kann – eine Verringerung der Hydroxidionen-Konzentration, also eine pH-Wertsenkung (ich will hier aber nicht zum übereiligen Einsatz pH-Wert-senkender Produkte anregen! – solche Maßnahmen müssen wohl überlegt sein, damit der pH-Wert am Ende noch im tolerierten Bereich für die Fische liegt).
Man kann diesen Sachverhalt auch grafisch darstellen. Im untenstehenden Diagramm habe ich den prozentuellen Anteil an Ammoniak am Gesamtstickstoff (hier die Summe aus Ammoniak und Ammonium) in Abhängigkeit des pH-Wertes dargestellt. Man sieht, dass bei Überschreiten eines kritischen pH-Werts die Ammoniakkonzentration schnell stark ansteigt!
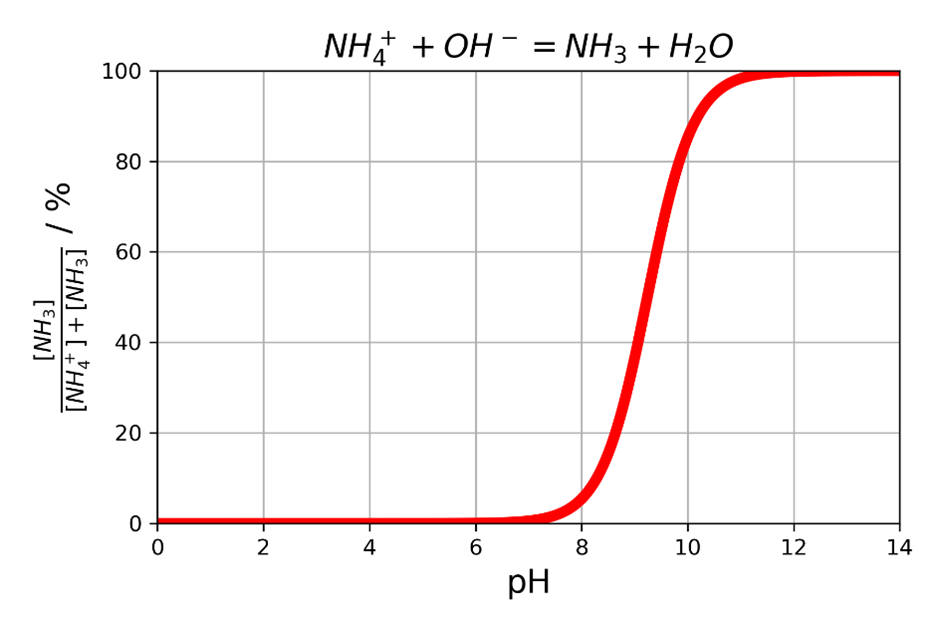
Eine weitere Variante ist, Ammoniumionen aus dem Gleichgewicht zu entfernen. Die Überlegung dabei ist dieselbe, wie gerade für den pH-Wert beschrieben. In Aquarien erfolgt das normalerweise gut, indem nitrifizierende Bakterien das Ammonium über Nitrit zu Nitrat abbauen. In neuen Becken und wenn der Filter keinen intakten Biofilm enthält, kann dieser Abbau jedoch eingeschränkt sein.
Warum Ammoniak für Fische giftig ist und wie es zu einer Ammoniakvergiftung von Fischen kommt [1, 2]
Die Hauptquelle von Ammoniak in Fischen selbst ist die Verstoffwechselung von Proteinen, die sie als Nahrung aufnehmen. Es wird angenommen, dass im Fall der Süßwasserfische etwa 90% der Ammoniakausscheidung über die Kiemen erfolgt. Voraussetzung für eine effiziente Abgabe aus dem Blut über die Kiemen in das Wasser ist aber ein ausreichender Konzentrationsunterschied, der nämlich die Triebkraft für die Ausscheidung aus dem Fisch ist. Wenn im Wasser bereits zu viel Ammoniak vorhanden ist, wird die Abgabe stark gehemmt. Saurere Wässer unterstützen also die Ausscheidung von Ammoniak, weil dieser im Wasser schnell zu Ammoniumionen reagiert (siehe Grafik oben). Fische versuchen im Fall erhöhter Ammoniakgehalte im Wasser die Ausscheidung durch größeren Durchfluss durch die Kiemen zu erhöhen. Das ist auch der Grund, warum an Ammoniakvergiftung verendete Fische die Kiemendeckel weit aufgestellt haben. Das Wirkprinzip der Ammoniak-Toxizität ist ziemlich kompliziert und wird auf die schädliche Einwirkung auf das zentrale Nervensystem zurückgeführt. Neben den Ausscheidungen der lebenden Fische, kommt Ammonium vor allem durch den Abbau von Biomasse in das Wasser.
Wie kann ich wissen, ob die Fische in meinem Teich oder Aquarium gefährdet sind?
Die Toxizität hängt neben Druck, Temperatur und Salinität hauptsächlich vom pH-Wert ab. Eine Analyse besteht daher sinnvollerweise aus der Bestimmung des Ammonium-Gehaltes und des pH-Wertes. Temperatur und Luftdruck werden bei den instrumentellen Analysen durch Moll Chemie standardmäßig zu Kompensationszwecken mitbestimmt. In Salzwasseraquarien kann zusätzlich eine Salinitätsbestimmung (Messung der elektrischen Leitfähigkeit) sinnvoll sein. Aus dem Ammonium-Gehalt und dem pH-Wert kann der Gehalt an toxischem Ammoniak im Wasser berechnet werden.
Vorsicht vor Ammoniak beim Desinfizieren von Teichen mit Branntkalk!
Gängige Praxis zur Desinfektion von Fischteichen ist eine Behandlung mit Branntkalk (CaO). Kommt Branntkalk mit Wasser in Kontakt, bildet sich Calciumhydroxid, das stark basisch ist. Darauf beruht auch die desinfizierende Wirkung. Die chemische Reaktion schaut so aus:
„Löschen“ des Kalkes (Reaktion mit Wasser):
CaO + H2O ⇌ Ca(OH)2
Dissoziation des Calciumhydroxids:
Ca(OH)2 ⇌ Ca2+ + 2 OH–
Es kommen dadurch also eine große Menge Hydroxidionen ins Wasser. Wenn der pH-Wert des Wassers nach einer Branntkalkbehandlung nicht genau kontrolliert wird, riskiert man eine akute Ammoniakvergiftung der (Wieder-)eingesetzten Fische, weil durch den hohen pH-Wert das Ammonium/Ammoniak-Gleichgewicht stark zu Gunsten des Ammoniaks liegt!
Gerne unterstütze ich Sie bei der Kontrolle auf unkritische Ammoniakwerte in Ihrem Teich oder Aquarium, um eine Ammoniakvergiftung von Ihren Fischen zu vermeiden! Schreiben Sie mir einfach über das Kontaktformular oder senden Sie mir eine Mail.
Quellen:
[1] Ip, Y. K; et. al.: Ammonia toxicity, tolerance, and excretion; Fish Physiology (2001)
[2] Randall, D. J.; et. al.: Ammonia toxicity in fish; Marine Pollution Bulletin (2002)

